Abordaje de “Guante Blanco” para resección de adenomas hipofisarios.
RESUMEN
Introducción: La técnica endoscópica endonasal ha evolucionado con gran celeridad en los últimos 20 años. Se desarrollaron desde un abordaje mono-nostril respetando las estructuras nasales hasta un abordaje bi-nostril con luxación/remoción de estructuras nasales y tallado de flaps. Tanto en la literatura, como en las reuniones científicas, se planteó una gran controversia respecto a cuál debe ser la dimensión de un corredor quirúrgico adecuado. La respuesta más equilibrada a dicha controversia, podría ser el presente abordaje de “Guante Blanco”. El objetivo del presente trabajo es describir la técnica quirúrgica paso a paso.
Materiales y Métodos: Para identificar reparos anatómicos claves a la hora de diseñar el abordaje en espécimen cadavérico se utilizaron 10 cabezas: 5 fijadas con técnica fresh-frozen y 5 fijadas con formol. Para describir la técnica quirúrgica paso a paso en una cirugía real se utilizaron videos quirúrgicos y protocolos de pacientes operados en Tucumán, entre enero de 2020 y enero de 2022.
Resultados: Se describe paso a paso con todos sus trucos este abordaje por vía baja, endoscópico, 1 ½ nostril, con máxima preservación anatomo-funcional nasal, trans-esfenoidal, trans-selar.
Conclusión: Se presentó e ilustró paso a paso este abordaje de “Guante Blanco”, de modo tal que pueda ser reproducido por el cirujano de base de cráneo en formación. Es sencillo, suficiente y rápido.
Palabras clave: Hipófisis. Adenoma. Abordaje endoscópico endonasal. Base de cráneo.
ABSTRACT
Introduction: The endonasal endoscopic approach has evolved fast in the last 20 years. It has evolved, from a mono-nostril approach respecting the nasal structures, to a bi-nostril approach with dislocation/removal of nasal structures and carving of flaps. In the literature and scientific meetings a great controversy arose regarding what the dimension of an adequate surgical corridor should be. The most balanced response to such controversy might be the present "Guante Blanco" approach. The objective of this paper is to describe this surgical technique step by step.
Materials and Methods: Pictures of dissected cadaveric specimen (five fixed with the fresh-frozen technique and five fixed with formalin) were used to identify key anatomical landmarks and design the technique. To describe the surgical aproach step by step in a real surgery, surgical videos and protocols of patients who have undergone surgery in Tucumán between January 2020 and January 2022, were included.
Results: This endonasal endoscopic approach, one and half nostril, with maximum anatomical-functional nasal preservation, trans-sphenoidal, trans-sellar is described step by step with all the author tricks and pearls.
Conclusion: The "Guante Blanco" approach is a simple, adequate, and fast surgical technique. This paper presented and illustrated this approched step by step in order to help skull base surgeon in training to reproduce it.
Keywords: Pituitary. Adenoma. Endoscopic endonasal approach. Skull base.
INTRODUCCIÓN
Los adenomas pituitarios son generalmente neoplasias benignas, con una prevalencia que va de 1/865 a 1/2688 individuos. En los últimos años la tasa diagnóstica ha ido aumentando en virtud de los avances de las técnicas neuroradiológicas: la incidencia de un adenoma es aproximadamente del 10% en RM.1 Parte de los pacientes con esta patología requieren tratamiento quirúrgico según estrictas indicaciones.2 Actualmente, la mayoría de éstos se pueden resolver por vía endoscópica endonasal.
La técnica endoscópica endonasal ha evolucionado con gran celeridad en los últimos 20 años. Se desarrollaron desde abordajes conservadores, mono-nostril respetando las estructuras nasales3, hasta abordajes bi-nostril con luxación/remoción de estructuras nasales y tallado de flaps.4 En las reuniones científicas contemporáneas se planteó una gran controversia respecto a cuál debe ser la dimensión de un corredor quirúrgico adecuado. La respuesta más equilibrada a dicha controversia podría ser el presente abordaje de “Guante Blanco”.
El propósito del presente trabajo es describir la técnica quirúrgica paso a paso.
MATERIALES y MÉTODOS
Para identificar reparos anatómicos claves a la hora de diseñar el abordaje en espécimen cadavérico se utilizaron 10 cabezas: 5 fijadas con técnica fresh-frozen y 5 fijadas con formol. A fines de objetivar adecuadamente la arteria esfenopalatina y sus ramas a través de la mucosa del receso esfeno-etmoidal se realizó una inyección de silicona coloreada siguiendo los lineamientos de la Escuela Anatómica de Viena. La misma consiste en una técnica muy similar a la descripta por Van Loveren5, pero con una modificación en la cantidad de catalizador (Christoph Fuchssteiner, comunicación personal). Este detalle en la técnica de inyección es el que modifica la viscosidad de la silicona y permite que la misma llegue a los vasos de menor calibre.
Para describir la técnica quirúrgica paso a paso en una cirugía real se utilizaron videos quirúrgicos y protocolos de pacientes operados en Tucumán, entre enero de 2020 y enero de 2022. Todas las cirugías fueron realizadas por el mismo equipo quirúrgico (AC-JFV-AMF). Las imágenes extraídas de dicho video fueron editadas en Power Point.
RESULTADOS
Técnica quirúrgica
La descripción paso a paso del abordaje incluye: el posicionamiento, la fase naso-esfenoidal, la fase selar hasta el momento previo a durotomía y una reseña sobre el cierre (fase reconstructiva).
Este procedimiento se efectúa con un endoscopio como elemento de visualización, sin necesidad de utilizar un retractor de Killian, ni otro similar.6,7
Paciente en posición semisentado con cabezal fijo de 3 pines. El ápex nasal del paciente debe estar enfrentado con el cirujano. La pantalla, la nariz del paciente y las manos del cirujano deben mantener un mismo eje; esto optimiza la ergonomía. Es clave considerar el concepto del punto esfeno-selar.8 Esta posición permite un campo exangüe, ergo una cirugía prolija.9
Se colocan cotonoides embebidos en adrenalina (concentración 1:1000) para topicar la mucosa de ambas fosas nasales. Esto se realiza antes de colocar campos, esperando la adecuada acción del vasoconstrictor.
Se introduce en la fosa nasal derecha una óptica endoscópica de cero grados, de 175 mm de longitud y 4 mm de diámetro. Se identifican de rutina las principales referencias anatómicas: el cornete inferior hacia lateral, el septum nasal hacia medial y el techo de la coana hacia posterior e inferior. La visualización del ostium esfenoidal es inconstante, ya que puede estar oculto por la mucosa o el cornete superior.
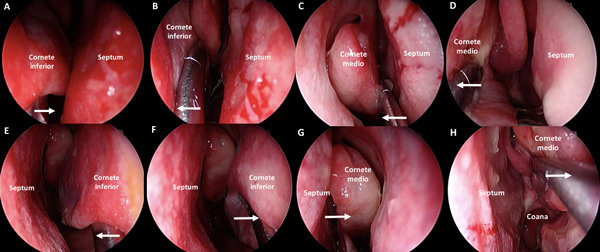
Se procede a la luxación hacia medial y desplazamiento hacia lateral de ambos cornetes inferiores. Luego, se coloca cotonoide embebido en vasoconstrictor entre el cornete medio y el septum nasal a cada lado. Acto seguido, con un disector de Cottle, se desplaza con delicadeza cada cornete medio hacia lateral. El cornete medio no debe ser resecado ni fracturado. Esta maniobra genera un corredor quirúrgico que permite el acceso al receso esfeno-etmoidal a cada lado (Figura 1 A-H).

Figura 1. Fase nasal: tratamiento de los cornetes. A-D: fosa nasal derecha. A-B: lateralización de cornete inferior derecho. C-D: lateralización de cornete medio derecho. E-H: fosa nasal izquierda. E-F: lateralización de cornete inferior izquierdo. C-D: lateralización de cornete medio izquierdo.
El próximo paso es identificar el ostium esfenoidal del lado derecho. Si el mismo no es visible, la maniobra más recomendada para identificarlo es utilizar un disector de Cottle para lateralizar el cornete superior en la unión de su tercio medio y posterior. Si aun así no logra identificarse, se procede palpando sin presionar demasiado en esta región hasta identificar una zona débil fenestrando delicadamente la mucosa. Se realiza finalmente un movimiento rotacional con el disector para ampliarlo (Figura 2 A-B).
La zona más baja del ostium coindice con el “punto de Cappabianca”, 12 mm por arriba del techo de la coana.10 (Figura 3 A-D) A partir de este punto comenzamos el tallado de un “mini-rescue flap” septal del lado derecho. Utilizamos una punta de colorado de 45 grados a tales efectos. Se trata de una modificación del rescue flap que utiliza el equipo de Ohio11; el corte anterior se efectúa buscando la proyección de la unión osteo-cartilaginosa septal (Figura 2 C-E).
Una vez expuesta esta región, se realiza con un disector presión sobre la misma, buscando la desinserción osteo-cartilaginosa (Figura 2F).
Acto seguido, se realiza una pequeña ventana en la parte posterior del septum a expensas del segmento óseo con una pinza punch. Es una mínima ventana que tiene como único objetivo permitir el acceso de instrumental a través de la otra fosa nasal (Figura 2G). Se utiliza de este modo 1 narina (la derecha) y ½ (izquierda). Se procederá entonces a identificar el ostium esfenoidal contralateral utilizando la técnica antes descripta. Se objetivan así, ambos ostium y la quilla esfenoidal (Figura 2H).
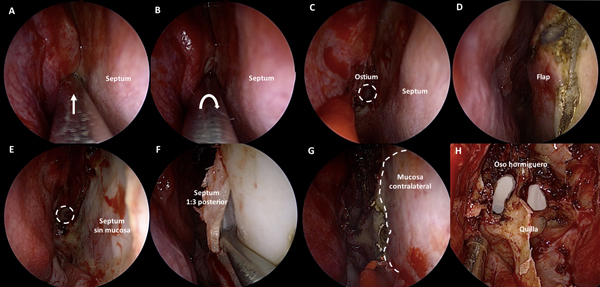
Figura 2. Fase naso-esfenoidal. A-B: identificación mediante palpación y apertura con maniobra rotacional del ostium esfenoidal. C-D: tallado del mini-rescue flap. E-F: septum denudado y desinserción osteo-cartilaginosa. G: exposición de mucosa contralateral luego de septectomía posterior; en línea de puntos se delimita el sitio de corte. H: rostro de oso hormiguero luego de exponer el rostrum esfenoidal.
Se procede a la apertura del rostrum esfenoidal, la cual debe ser siempre amplia. Muchas veces es esto lo que proporciona un adecuado surgical freedom y no la amputación de estructuras nasales. Luego, se resecan todos los septos intrasinusales y se exentera la mucosa a fines de exponer con claridad todos los reparos anatómicos: la prominencia del piso de la silla turca al centro, la silueta de ambas arterias carótidas internas a los lados, el planum esfeno-etmoidal arriba y el clivus abajo (Figura 4 A-B).
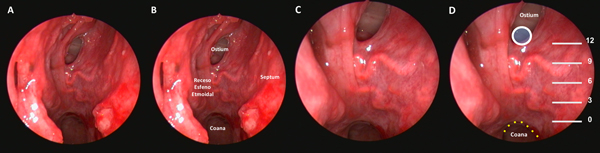
Figura 3. Preparado cadavérico que muestra reparos a la hora de tallar el mini-rescue flap. A: receso esfeno-etmoidal. B: ídem a A con nomenclatura. C: zoom para evidenciar arteria esfenopalatina en receso esfeno-etmoidal. D: correlación entre el punto de Cappabianca (circulo celeste con borde blanco) y el borde inferior del ostium esfenoidal.
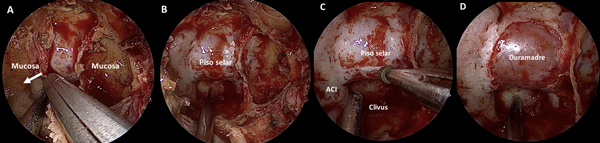
Figura 4. Tiempo intrasinusal. A-D: exposición de la duramadre selar.
En este momento de la cirugía se suma un cirujano más; entonces uno de ellos maneja el endoscopio dinámicamente y otro el instrumental con ambas manos utilizando “1 y ½ fosa nasal” (i.e. 3-4 hands technique)12. El endoscopio es sostenido por un cirujano asistente en la fosa nasal derecha, hacia arriba (a horas 12.00). El cirujano principal sostiene un instrumento con cada mano: con la mano izquierda generalmente un cánula de aspiración de Frank-Pasquini que ingresa por la fosa nasal derecha sin entrar en conflicto con la óptica (a horas 06.00), y con la mano derecha el instrumento principal que va cambiando según el momento (e.g. bisturí, curetas, entre otros).13
En la fase selar la pared posterior del seno esfenoidal (i.e la prominencia selar) es fresada con punta diamantada a fines de disminuir su espesor (Figura 4C). Luego, se realiza una apertura “a medida” utilizando una pinza de Kerrison N°1. El plano dural queda expuesto hasta evidenciarse los “cuatro azules” o la “corona azul” (i.e. el limite más medial de ambos senos cavernosos y el límite de ambos senos intercavernosos)14 (Figura 4D).
En el tiempo intradural de la fase selar (que no es parte del abordaje) se efectúa la resección tumoral. Luego de finalizar con la resección tumoral se realiza “diving technique” (i.e. técnica de buceo) para chequear la hemostasia.15 Finalmente se evalúa el subtipo intraoperatorio de barrera selar16 y la presencia o no de fistula de LCR; que en caso de producirse, la misma se categorizará según la clasificación de Esposito-Kelly17.
Ante la presencia de fistula de LCR, el mini rescue flap se transforma en un flap naso-septal y se procede a cierre con “técnica de 3F” (i.e. fat, flap, flash)18. Esto último implica colocación de grasa, cola de fibrina y flap; movilizando al paciente de forma temprana en el post-operatorio inmediato. En caso de no producirse fistula de LCR (escenario más probable por la selección de pacientes) se prosigue con el cierre.
Finalmente, se chequea hemostasia en ambas fosas nasales, se reposiciona el colgajo septal de rescate y el cornete medio es delicadamente restituido a su posición inicial. Se colocan splits nasales para evitar sinequias futuras. Finalmente, se procede a la aspiración faríngea (sangre, saliva y líquido de lavado), ya que el packing de esta región no se realiza de rutina.
DISCUSIÓN
Breve reseña histórica de la cirugía endoscópica hipofisaria
El endoscopio fue introducido en la cirugía de la hipófisis en 1963 por Gerard Guiot et al.19 Sin embargo, la idea permaneció sin reconocer hasta la contribución adicional de Apuzzo et al.20 en 1977. Su uso se desarrolló aún más gracias a los avances técnicos de las ópticas. Sin embargo, el endoscopio fue adoptado sólo en casos seleccionados para complementar el microscopio en las primeras o últimas etapas de un procedimiento tradicional, determinando el primer ejemplo de técnica "asistida por endoscopio".21 Por su parte, Jho y Carrau et al.22,23 fueron los primeros en describir en detalle una técnica endoscópica endonasal transesfenoidal "pura". Desde entonces, el abordaje endoscópico endonasal (AEE) se ha utilizado en todo el mundo en la resección de adenomas pituitarios.
Evolución del abordaje endoscópico endonasal y su relación con la preservación nasal.
En un primer tiempo, se desarrolló el FEPS (i.e. functional endoscopic pituitary surgery), un abordaje endoscópico estándar para el tratamiento de las lesiones infradiafragmáticas. El mismo utilizaba una sola narina (i.e. mono-nostril) y no requería la remoción de ninguna estructura nasal.3
Luego, se desarrolló una técnica dinámica. La misma requería utilizar ambas fosas nasales (i.e. bi-nostril), la luxación lateral bilateral de los cornetes medios y la remoción del sector posterior del tabique nasal.24
Más adelante, se desarrolló el abordaje endoscópico endonasal extendido. Esto llevó al equipo de Pittsburgh a establecer el paradigma de que “una mayor remoción de estructuras nasales logra una exposición mayor y un adecuado surgical freedom”. El mismo incluyó la turbinectomía media uni y/o bilateral, la etmoidectomía anterior y posterior uni y/o bilateral, combinada con una septectomía posterior más grande y una esfenoidotomía más amplia.25,26 Además, se debe tener en cuenta que el abordaje extendido implica muchas veces el uso de flap naso-septal para reparar el amplio defecto osteo-dural. Esto se logra a expensas de una amplia disección de la mucosa del tabique nasal.27
El neurocirujano en formación no debe ser ajeno a las complicaciones nasales que puede generar el tallado de un flap naso-septal, tales como: perforación septal, absceso para-septal, epistaxis, trastornos ventilatorios, déficit en la olfacción, entre otros.28
Al realizar un análisis de lo expresado hasta este punto llama la atención que mientras la técnica endoscópica endonasal evolucionaba, la preservación de la mucosa nasal fue involucionando. Esto devino, en los últimos años, en la controversia respecto a la amplitud adecuada del corredor nasal. Dicho de otro modo, se puso en discusión cuán agresiva debe ser la remoción de estructuras nasales para generar un corredor quirúrgico suficiente. El análisis del surgical freedom y la extensión del corredor endonasal reveló que no siempre se justifica la extensa resección de las estructuras paranasales.29 Debe considerarse que a mayor resección/manipulación de estructuras, mayor morbilidad funcional nasal, mayor tiempo de recuperación, y mayor posibilidad de complicaciones.
Guante Blanco: origen de la técnica e influencias.
Por lo expresado en el apartado precedente es lógico deducir que la próxima técnica a desarrollarse debía ofrecer un corredor quirúrgico adecuado para conseguir la máxima resección tumoral posible y permitida, así como la máxima indemnidad posible de las estructuras nasales. La próxima técnica a desarrollarse debía ser un punto intermedio entre el mono-nostril y el bi-nostril, entre la indemnidad casi absoluta y la resección agresiva de estructuras nasales. Debía ser una técnica “equilibrada”.
En la Escuela de Nápoles, donde se realiza un estudio del proceso evolutivo de las técnicas endoscópicas de base de cráneo, el último autor (DS) fue quien estableció las bases de una nueva técnica. El mismo ideó un abordaje 1 ½ nostril con máxima preservación de los cornetes y mínima alteración del tabique nasal, sin tallado de flaps definitivos de modo sistemático.
El primer autor (JFV) tomó dicha técnica y le realizó una serie de modificaciones influenciado por otras Escuelas:
A este nuevo abordaje con sus modificaciones lo denominamos “Guante Blanco” (i.e. Guanti Bianchi en italiano).
Indicaciones de “Guante Blanco”
La técnica de “Guante Blanco” se indica en pacientes con macroadenomas no funcionantes, apoplejía pituitaria, enfermedad de Cushing, acromegalia, adenoma secretor de TSH y en portadores de prolactinomas con una clara indicación quirúrgica. La indicación principal es en tumores infradiafragmáticos, es decir, por debajo de la duramadre del diafragma selar o respetando el orificio del anillo dural (Figura 5). Se podría valorar a futuro su indicación en casos con extensión supraselar sin invasión ventricular y sin invasión lateral.
Existen situaciones que contraindican relativamente el uso de esta técnica y precisa un abordaje “extendido”: adenoma en reloj de arena, alto grado de extensión supraselar (e.g. invasión del III ventrículo), extensión para-selar (e.g. englobamiento carotideo), consistencia dura o fibrosa del tumor (Figura 6).
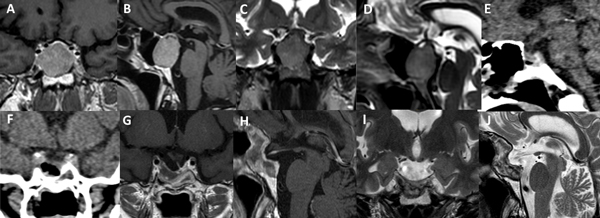
Figura 5. Paciente de 45 años con prolactinoma infradiafragmático resistente a cabergolina. Se utilizó un abordaje de Guante Blanco para su tratamiento. A-D: RM preoperatoria. E-F: TC del primer día postoperatorio. G-J: RM postoperatoria.
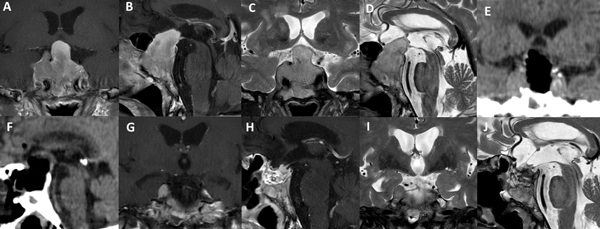
Figura 6. Paciente de 62 años, acromegálica, con adenoma gigante Hardy C y Knosp 4. No fue candidata a abordaje de Guante Blanco. Se utilizó un abordaje extendido para su tratamiento. A-D: RM preoperatoria. E-F: TC del primer día postoperatorio. G-J: RM postoperatoria.
Un poco de historia
El nombre de esta nueva técnica surgió tras plantear una analogía con un famoso robo. En 1911 el dúo italo-argentino integrado por Vincenzo Peruggia (actor material) y el marqués Eduardo Valfierno (actor intelectual) robaron la Mona Lisa del Museo del Louvre sin violencia y sin dejar rastro.32 Si la fosa nasal es el Louvre, el adenoma hipofisario es la Mona Lisa, el neurocirujano debe comportarse como un verdadero ladrón de “Guante Blanco”, sin dejar ningún rastro (Figura 7).

Figura 7. El semanario italiano de la época, La Domenica del Corriere, muestra en su portada una ilustración del robo (al centro). En sus páginas pueden objetivarse los dibujos de una secuencia del hecho (izquierda) y una famosa fotografía que muestra el espacio vacío en la pared sin el cuadro (derecha).
CONCLUSIÓN
Se presentó e ilustró paso a paso este abordaje de “Guante Blanco”, de modo tal que pueda ser reproducido por el cirujano de base de cráneo en formación. Se trata de un abordaje por vía baja, endoscópico, 1 ½ nostril, con máxima preservación anátomo-funcional nasal, trans-esfenoidal, trans-selar. Es sencillo, suficiente y rápido. “Lo bueno, si breve, dos veces bueno”.
BIBLIOGRAFÍA
COMENTARIO
Se trata de un artículo interesante que analiza en detalle los abordajes transnasales para el tratamiento de los adenomas de hipófisis, describe la técnica guante blanco que intenta preservar al máximo las estructuras nasales, sin abandonar la técnica de 4 manos. Esta técnica podría resultar útil con el objeto de disminuir la morbilidad postoperatoria nasal, costras post operatorias o alteraciones en la circulación del aire y mejorar los tiempos quirúrgicos que suelen prolongarse con el tallado del colgajo nasoseptal completo de manera sistemática.
La técnica se describe en detalle lo que resulta útil para aquellos que están iniciando su experiencia en cirugía endoscópica transnasal.
Cabe destacar que en algunos casos la anatomía nasal puede dificultar este acceso y que la resección del cornete medio uni o bilateral no debería generar gran morbilidad, por lo menos en nuestra experiencia.1
En relación con el colgajo de rescate, se describe muy bien cómo preservar su irrigación. En este sentido, cabe recordar que la arteria septal posterior rama de la esfeno palatina se encuentra aproximadamente a 1.5 cm del borde superior de la coana.2,3
Finalmente, felicito a los autores que buscan de manera constante mejorar los resultados quirúrgicos sobre bases científicas, objetivo fundamental de nuestra especialidad.
Pablo Ajler
Jefe del Servicio de Neurocirugía
Hospital Italiano de Buenos Aires
BIBLIOGRAFÍA
COMENTARIO
Los autores describen una técnica quirúrgica que denominaron “Guante Blanco” (en analogía con el famoso robo de la Mona Lisa del Museo del Louvre) para realizar el abordaje endoscópico endonasal para el tratamiento quirúrgico de los adenomas hipofisarios (AH). Es un abordaje sin resección ni luxación de estructuras nasales que les permite obtener un corredor quirúrgico rinosinusal suficiente para la resección de la mayoría de los AH. Describen el paso a paso de la técnica en especímenes anatómicos y en imágenes quirúrgicas, con los tips en cada una de sus fases.
Existe una gran controversia sobre la extensión del abordaje transnasal requerido para la resección de un AH, yendo desde el uninostril sin resección de estructuras nasales hasta el binostril con resección de cornetes, etmoidectomía y tallado de flaps. Hay escuelas que propugnan abordajes más invasivos con el objetivo de obtener corredores más amplios para facilitar y maximizar la resección quirúrgica, principalmente en adenomas grandes y gigantes. Los defensores de los abordajes menos invasivos hacen hincapié en la morbilidad rinosinusal que provoca la resección de las estructuras nasales y el tallado de los flaps.
Personalmente, creo que uno no debe ser dogmático ni estructurado a la hora de elegir un determinado abordaje. Debemos tener la suficiente versatilidad para seleccionar el abordaje transnasal individualizado y a medida para cada paciente, teniendo en cuenta la anatomía nasal, sinusal y esfenoidal (espolones anteriores y posteriores, desviaciones septales, cornetes bullosos, hipertrofia de cornetes, etc) como así también el tipo de tumor (tamaño, extensión, consistencia) a tratar. También considero de vital importancia trabajar en equipo con un otorrinolaringólogo experto en cirugía endoscópica rinosinusal, tanto para diseñar, planificar y realizar el abordaje específico para cada paciente, como así también para el manejo postoperatorio (necesidad de limpieza nasal con debridamiento, remoción de costras, liberación de sinequias, reparación de defectos septales, etc) y de esta forma reducir la morbilidad rinosinusal.
Felicito a los autores por la presentación de este trabajo bien escrito y documentado que seguramente servirá de guía para los neurocirujanos en formación en endoscopía de base de cráneo.
Dr Martín Guevara Mendez
Jefe Unidad Neurocirugía Hospital Fernandez
Jefe Sección Neurocirugía CEMIC